I. ĐỒNG ĐẰNG, ĐỒNG PHÂN, DANH PHÁP
1. Đồng đẳng
Bạn đang xem: Lý thuyết ankan | SGK Hóa lớp 11
- Công thức tổng quát tháo công cộng mang đến ankan là CnH2n+2 (n ≥ 1).
- Tên gọi công cộng là ankan hoặc paraffin.
- Công thức đơn giản và giản dị nhất là metan (CH4).
- Mạch cacbon hở, rất có thể phân nhánh hoặc ko phân nhánh.
- Trong phân tử chỉ mất links đơn (liên kết, …) tạo ra trở thành kể từ 4 obitan lai hóa sp3 của vẹn toàn tử cacbon, kim chỉ nan loại tứ diện đều. Do tê liệt mạch cacbon sở hữu dạng hấp tấp khúc. Các vẹn toàn tử cacbon rất có thể xoay kha khá tự tại xung xung quanh những links đơn.
2. Đồng phân
Ankan chỉ mất đồng phân mạch C Khi sở hữu kể từ 4C trở lên trên.
Ví dụ: Các đồng phân của C5H12.
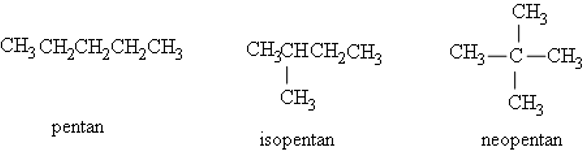
3. Danh pháp
– Phân tử sở hữu mạch nhánh thì gọi theo dõi quy tắc sau:
+ Chọn mạch chính: là mạch nhiều năm nhất có tương đối nhiều group thế nhất.
+ Đánh số địa điểm cacbon vô mạch chủ yếu chính thức kể từ phía sát nhánh rộng lớn.
+ Gọi tên: Vị trí mạch nhánh + thương hiệu nhánh + thương hiệu mạch chủ yếu (tên ankan ứng với số vẹn toàn tử cacbon vô mạch chính).
*Lưu ý:
- Tên thường:
+ Nếu chỉ tồn tại một nhánh có một không hai CH3 ở vẹn toàn tử C số 2 thì tăng chi phí tố iso.
+ Nếu sở hữu 2 nhánh CH3 ở C số 2 thì tăng chi phí tố neo.
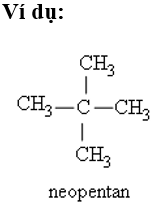
- Gốc hiđrocacbon là phần còn lại của phân tử hidrocacbon sau khoản thời gian ngắn hơn một trong những vẹn toàn tử hiđro tuy nhiên vẫn còn đấy tồn tại vô phân tử ở hiện trạng links và ko đem electron tự tại như gốc tự tại.
- CTTQ group ankyl: CnH2n+1
- Bậc của một vẹn toàn tử cacbon vô phân tử ankan thông qua số vẹn toàn tử cacbon links thẳng với nó.
II. TÍNH CHẤT VẬT LÍ
- Tại ĐK thông thường ankan kể từ C1 → C4 ở hiện trạng khí, kể từ C5 → C17 trở lên đường ở hiện trạng lỏng, kể từ C18 trở lên trên ở dạng rắn. Nhiệt nhiệt độ chảy, sức nóng chừng sôi và lượng riêng rẽ của ankan rằng công cộng tăng theo hướng tăng của phân tử khối.
- Ankan là những hóa học ko màu sắc, ko tan nội địa, nhẹ nhàng rộng lớn nước tuy nhiên tan nhiều vô dung môi cơ học.
III. TÍNH CHẤT HÓA HỌC
Xem thêm: [ Tập Hợp] Những thông tin cần biết về Bệnh viện E
1. Phản ứng thế
- Nguyên tử H bị thế vày halogen tạo ra dẫn xuất halogen:
CnH2n+2 + x Cl2 → CnH2n+2-xClx + x HCl (x ≤ 2n+2)
- Đối với ankan phân tử sở hữu những vẹn toàn tử C sở hữu bậc không giống nhau, thành phầm chủ yếu thế H ở C bậc cao hơn nữa.
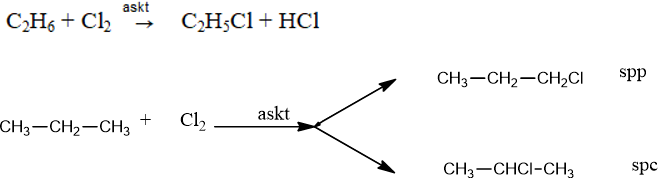
2. Phản ứng tách
- Tách hiđro (đề hiđro hóa): CnH2n+2 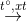 CnH2n+2-2x + xH2
CnH2n+2-2x + xH2
- Bẻ gãy những links C-C ( cracking): CnH2n+2 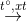 CmH2m + Cm’H2m’+2 (n = m + m’)
CmH2m + Cm’H2m’+2 (n = m + m’)
3. Phản ứng oxi hóa( nhóm cháy)
Ankan cháy tạo nên nhiều nhiệt:
CnH2n+2 + \(\dfrac{{3n + 1}}{2}\) O2 → n CO2 + (n+1) H2O
Nhận xét:
+ Đốt ankan thu nCO2 < nH2O
+ Nếu nhóm hiđrocacbon chiếm được nCO2 < nH2O ⇒ Hiđrocacbon rước nhóm là ankan (CnH2n+2).
IV. ĐIỀU CHẾ
- Trong công nghiệp, metan và những đồng đẳng được lấy kể từ khí vạn vật thiên nhiên, khí mỏ dầu và dầu lửa.
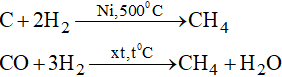
- Trong chống thí nghiệm, ankan được pha trộn bằng phương pháp nung muối hạt natri của axit cacboxylic với vôi tôi xút.
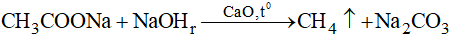
V. ỨNG DỤNG
- Dùng thực hiện nhiên liệu vô hàn hạn chế sắt kẽm kim loại.
- Dùng thực hiện dầu chất bôi trơn, dung môi.
- Để tổ hợp nhiều hóa học cơ học khác: CH3Cl, CH2Cl2, CCl4, CF2Cl2, ...
- điều đặc biệt kể từ CH4 điều chế được rất nhiều hóa học không giống nhau: láo lếu thích hợp CO + H2, ammoniac, C2H2, rượu metylic, andehit fomic, …
Xem thêm: Top 10+ trang web AI vẽ tranh cực đỉnh, không thể bỏ qua 2024
Sơ đồ gia dụng tư duy: Ankan
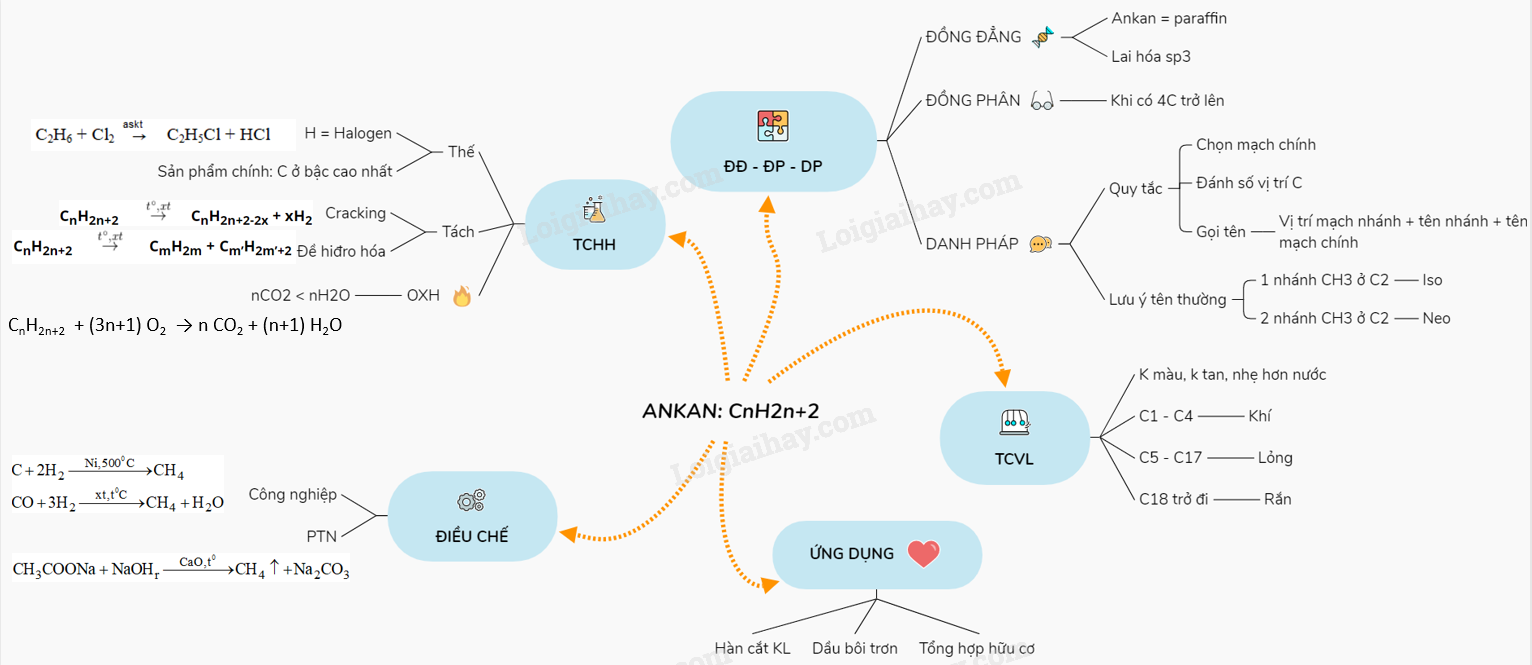
Loigiaihay.com