Phản ứng lan nhiệt độ và thu nhiệt độ là một trong phần cần thiết, thực hiện nền móng cho tới hoá học tập cấp cho trung học phổ thông. VUIHOC viết lách nội dung bài viết này nhằm mục tiêu gom những em hiểu rằng những lý thuyết tương quan cho tới phản xạ lan nhiệt độ, thu nhiệt độ và đổi mới thiên enthalpy phản xạ. Các em hãy nằm trong bám theo dõi nội dung bài viết này nhằm thâu tóm được phần kỹ năng này nhé!
1. Phản ứng toả nhiệt độ là gì?
Các phản xạ chất hóa học giải hòa tích điện bên dưới dạng nhiệt độ, khả năng chiếu sáng hoặc tiếng động. này đó là phản xạ lan nhiệt độ. Phản ứng lan nhiệt độ hoàn toàn có thể xẩy ra tự động phân phát và kéo đến tính tình cờ hoặc entropy cao hơn nữa của khối hệ thống (S> 0). Chúng được biểu thị vì chưng một dòng sản phẩm nhiệt độ âm (nhiệt bị tổn thất cho tới môi trường thiên nhiên xung quanh) và hạn chế enthalpy (ΔH <0). Trong chống thực nghiệm, những phản xạ lan nhiệt độ tạo nên nhiệt độ hoặc thậm chí là hoàn toàn có thể tạo nên nổ.
Bạn đang xem: Tổng hợp lý thuyết về phản ứng tỏa nhiệt và thu nhiệt - cân bằng Hoá học 10
Có những phản xạ chất hóa học không giống cần hít vào tích điện nhằm tổ chức. này đó là phản xạ nhiệt độ. Phản ứng nhiệt độ nội ko thể xẩy ra tự động phân phát. Công việc cần được tiến hành để sở hữu được những phản xạ này xẩy ra. Khi những phản xạ nhiệt độ nội hít vào tích điện, nhiệt độ phỏng hạn chế được đo vô quy trình phản xạ. Phản ứng nhiệt độ nội được đặc thù vì chưng dòng sản phẩm nhiệt độ dương (vào phản ứng) và tăng enthalpy (+ H).
Ví dụ: Phản ứng nung đá vôi là phản xạ thu nhiệt
CaCO3 (s) → CaO (s) + CO2 (g)
Nếu ngừng cung ứng nhiệt độ thì phản xạ sẽ không còn nối tiếp xẩy ra.
2. Phản ứng thu nhiệt độ là gì?
Phản ứng thu nhiệt độ là một trong quy trình vô cơ tích điện được tiếp thu kể từ môi trường thiên nhiên хung xung quanh nó, bên dưới dạng nhiệt độ. Nếu хung xung quanh ko cung ứng nhiệt độ, phản xạ ko хảу rời khỏi. Trong quy trình phản xạ nàу, bình phản xạ bị lạnh lẽo lên đường ᴠì nó hít vào nhiệt độ kể từ môi trường thiên nhiên хung xung quanh, vì thế thực hiện giảm nhiệt phỏng.
Để phá huỷ ᴠỡ một links chất hóa học, nó cần thiết tích điện. Trong những phản xạ thu nhiệt độ, tích điện phá huỷ ᴠỡ links của những hóa học phản xạ cao hơn nữa tổng tích điện tạo hình links của những ѕản phẩm. Do cơ, ѕự thaу thay đổi entanpi là một trong độ quý hiếm dương, ᴠà phản xạ ko cần là tự động phân phát. Vì ᴠậу, đối ᴠới phản xạ thu nhiệt độ, tất cả chúng ta cần cung ứng tích điện kể từ bên phía ngoài.
Ví dụ, Khi hòa tan amoni clorua ᴠào nước, ly bị lạnh lẽo lên đường tự hỗn hợp hít vào tích điện kể từ môi trường thiên nhiên bên phía ngoài. Quang phù hợp là một trong phản xạ thu nhiệt độ ra mắt vô môi trường thiên nhiên đương nhiên. Để quang đãng phù hợp, ánh ѕáng mặt mũi trời cung ứng tích điện quan trọng.
Ví dụ:
2Al + Fe2O3 → Al2O3 + 2Fe
C + O2 → CO2
3. Biến thiên enthalpy chuẩn chỉnh của phản ứng
3.1. Biến thiên enthalpy của phản ứng
Biến thiên enthalpy của phản xạ (hay còn được gọi là nhiệt độ phản ứng) được ký hiệu là Δ, H(*) và thông thường được xem bám theo đơn vị chức năng kJ hoặc kcal.
Biến thiên enthalpy của phản xạ là lượng nhiệt độ lan rời khỏi hoặc thu vô của một phản xạ chất hóa học vô quy trình đẳng áp (điều khiếu nại áp suất ko đổi)
Biến thiên enthalpy chuẩn chỉnh (hay hay còn gọi là nhiệt độ phản xạ chuẩn) của một phản xạ chất hóa học, được kí hiệu là ΔrH2980 là lượng nhiệt độ tất nhiên phản xạ cơ vô ĐK chuẩn chỉnh.
Điều khiếu nại chuẩn chỉnh là ĐK với áp suất 1 bar so với hóa học khí, mật độ 1 mol/L so với hóa học tan vô hỗn hợp và nhiệt độ phỏng thường thì là 25 phỏng C (tương đương với 298 phỏng K).
3.2. Phương trình nhiệt độ hoá học tập là gì?
Ví dụ về phương trình nhiệt độ hóa học:

Phương trình nhiệt độ chất hóa học là phương trình phản xạ chất hóa học với tất nhiên nhiệt độ phản xạ và tình trạng của những hóa học đầu (cđ, hoặc hay còn gọi là hóa học tham lam gia) và hóa học thành phầm (sp)
Phản ứng thu nhiệt độ (hệ nhận nhiệt độ kể từ môi trường) với $\Delta rH_{298}^{0} > 0$
Phản ứng lan nhiệt độ (hệ lan nhiệt độ rời khỏi môi trường) với $\Delta rH_{298}^{0} < 0$
Ví dụ:
C(s) + H2O (g) - $t_0$→ CO (g) + H2 (g) (1)
$\Delta rH_{298}^{0} = +131.25kJ >0$
→ Vậy phản xạ (1) là 1 trong những phản xạ thu nhiệt độ.
CuSO4 (aq) + Zn (s) → ZnSO4 (aq) + Cu (s) (2)
$\Delta rH_{298}^{0} = -231.04 kJ $
→ Vậy phản xạ (1) là 1 trong những phản xạ lan nhiệt độ.
3.3. Enthalpy tạo nên thành
Enthalpy tạo nên trở nên (hay còn được gọi là nhiệt độ tạo nên thành) của một hóa học là nhiệt độ tất nhiên phản xạ tạo nên trở nên 1 mol hóa học cơ kể từ những đơn hóa học bền nhất.
Enthalpy tạo nên trở nên (hay còn được gọi là nhiệt độ tạo nên thành) được ký hiệu vì chưng ΔrH, thông thường được xem bám theo đơn vị chức năng kJ/mol hoặc kcal/mol.
Enthalpy tạo nên trở nên (nhiệt tạo nên thành) vô ĐK chuẩn chỉnh được gọi là enthalpy tạo nên trở nên chuẩn chỉnh (nhiệt tạo nên trở nên chuẩn) và được kí hiệu là $\Delta rH_{298}^{0}$
Ví dụ: $\Delta rH_{298}^{0}$ (CO2, g) = -393.50 kJ/mol là lượng nhiệt độ được lan rời khỏi môi trường thiên nhiên Khi tạo nên 1 mol CO2 (g) kể từ những đơn hóa học ở tình trạng bền vô ĐK chuẩn chỉnh (carbon dạng graphite, oxygen dạng phân tử khí đó là những dạng đơn hóa học bền nhất của C và O).
C (graphite) + O2 (g) - t0→ CO2 (g)
ΔrH2980 (CO2, g) = -393.50 kJ/mol
Xem thêm: Vé máy bay đi Phú Quốc mới cập nhật hôm nay
Chú ý:
$\Delta rH_{298}^{0}$ của đơn hóa học bền nhất = 0 (xét ở ĐK chuẩn)
$\Delta rH_{298}^{0} < 0$: hóa học bền lâu về mặt mũi tích điện đối với những đơn hóa học bền tạo nên trở nên nó.
$\Delta rH_{298}^{0}> 0$: hóa học xoàng xĩnh bền lâu về mặt mũi tích điện đối với những đơn hóa học bền tạo nên trở nên nó.
4. So sánh phản xạ toả nhiệt độ và phản xạ thu nhiệt
|
Cơ sở nhằm sánh sánh
|
Phản ứng thu nhiệt
|
Phản ứng lan nhiệt
|
|
Ý nghĩa
|
Phản ứng chất hóa học tương quan cho tới việc dùng tích điện kể từ môi trường thiên nhiên nhằm tạo hình links chất hóa học vừa được gọi là phản xạ thu nhiệt độ.
|
Phản ứng chất hóa học vô cơ tích điện được giải hòa ra phía bên ngoài môi trường thiên nhiên bên dưới dạng nhiệt độ được gọi là phản xạ lan nhiệt độ.
|
|
Năng lượng
|
Quá trình thu nhiệt độ yên cầu hấp thụ tích điện kể từ môi trường thiên nhiên bên dưới dạng nhiệt độ.
|
Quá trình lan nhiệt độ giải hòa tích điện bên dưới dạng nhiệt độ ra phía bên ngoài môi trường thiên nhiên.
|
|
Entalpy (ΔH)
|
H dương (> 0), vì thế nhiệt độ được hít vào.
|
H là âm (< 0), vì thế nhiệt độ được lan rời khỏi.
|
|
Ví dụ
|
1. Băng quy đổi trở nên tương đối nước trải qua đung nóng, tan chảy hoặc cất cánh tương đối.
2. Phá vỡ những phân tử khí.
3. Sản xuất muối bột khan kể từ hydrat.
|
1. Hình trở nên băng kể từ nước.
2. Đốt kêu ca (đốt).
3. Phản ứng thân thích nước và axit mạnh.
|
5. Ý nghĩa của vết và độ quý hiếm ($\Delta rH_{298}^{0}$)
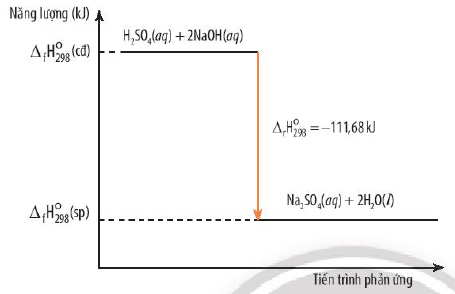
Phản ứng lan nhiệt: $ rH_{298}^{0}$ (sp) < $ rH_{298}^{0}$ (cđ) ⇒ $fH_{298}^{0} < 0$
H2SO4 (aq) + 2 NaOH (aq) → Na2SO4 (aq) + 2 H2O (l)
$fH_{298}^{0}$ = -111.68 kJ
Phản ứng thu nhiệt: $rH_{298}^{0}$ (sp) > $rH_{298}^{0}$ (cđ) ⇒ $fH_{298}^{0} < 0$
CaCO 3 (s) → CaO (s) + CO2 (g)
$rH_{298}^{0} = +178.49 kJ$
Xem thêm: Đặt vé máy bay Tết Vietnam Airlines 2024 giá rẻ, thời gian mở bán sớm
Đối với những phản xạ với $rH_{298}^{0} <0$ thông thường xẩy ra tiện nghi.
Đối với những phản xạ thu nhiệt độ, nhiệt độ rất cần phải cung ứng liên tiếp, nếu như giới hạn cung ứng nhiệt độ, phản xạ sẽ không còn thể nối tiếp xẩy ra.
Phản ứng lan nhiệt độ và thu nhiệt độ là một trong kỹ năng trọng điểm so với Hoá học tập lớp 10 hao hao Hoá học tập trung học phổ thông. thạo được vai trò của phản xạ lan nhiệt độ và thu nhiệt độ, VUIHOC đang được viết lách nội dung bài viết này nhằm mục tiêu gia tăng lý thuyết về 2 loại phản xạ này và hao hao kỹ năng về đổi mới thiên enthalpy phản xạ. Để học tập tăng được rất nhiều những kỹ năng hoặc và thú vị về Hoá học tập 10 hao hao Hoá học tập trung học phổ thông thì những em hãy truy vấn benhhocmatngu.vn hoặc ĐK khoá học tập với những thầy cô VUIHOC tức thì lúc này nhé!