I. KHÍ LÍ TƯỞNG (quan điểm vĩ mô)
Khí lí tưởng là hóa học khí tuân theo đuổi những tấp tểnh luật Boyle – Mariotte, Charles, Gay Lussac.
Bạn đang xem: 10.5.4. PHƯƠNG TRÌNH TRẠNG THÁI KHÍ LÍ TƯỞNG
II. PHƯƠNG TRÌNH TRẠNG THÁI KHÍ LÍ TƯỞNG
Xét một khối khí lí tưởng thay đổi kể từ tình trạng 1 (p1, V1, T1) quý phái tình trạng 2 (p2, V2, T2) trải qua tình trạng trung gian ngoan 1′ (p’, V’, T’) sao cho tới T’ = T1 và V’ = V2.
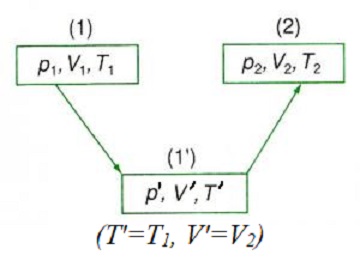
- Từ (1) → (1′) là quy trình đẳng sức nóng T’ = T1:
(*)
- Từ (1′) → (2) là quy trình đẳng tích V’ = V2:
(**)
(*) =>
(**) =>
Do đó:
(***)
Thay T’ = T1 và V’ = V2 vào (***) :
Vậy:
hằng số (const)
(phương trình tình trạng khí lí tưởng)
III. QUÁ TRÌNH ĐẲNG ÁP
3.1. Quá trình đẳng áp
Quá trình đẳng áp là quy trình thay đổi tình trạng nhập cơ áp suất không đổi.
3.2. Liên hệ thân thuộc thể tích V và sức nóng chừng vô cùng T nhập quy trình đẳng áp
Ta có:
hằng số (const) với p = hằng số (const)
Do đó:
hằng số (const)
(định luật Gay Lussac 2 #định luật Charles?)
3.1. Đường đẳng áp
Đường đẳng áp là đàng trình diễn sự trở nên thiên của thể tích theo đuổi sức nóng chừng Khi áp suất ko thay đổi.
Do nên
Xem thêm: Cách tải Shopee trên máy tính đơn giản cho người mới bắt đầu
(dạng y = a.x)
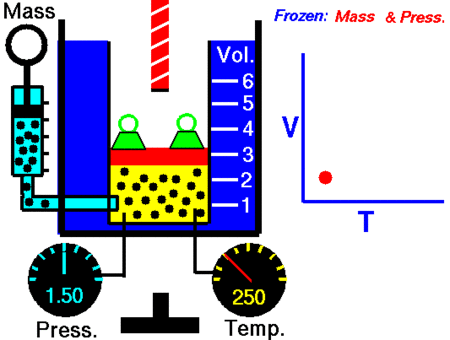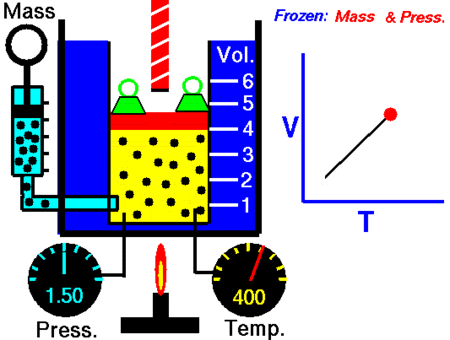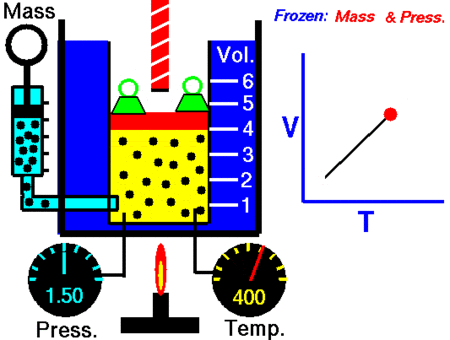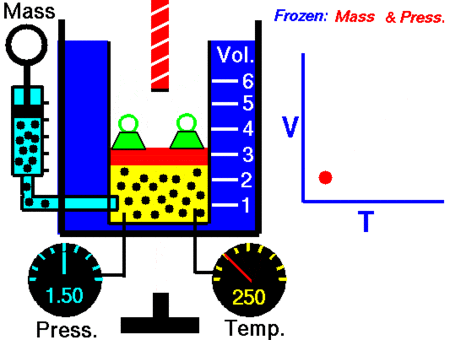
Trong hệ toạ chừng (V, T), đàng đẳng áp là đường thẳng liền mạch sở hữu đàng kéo dãn dài trải qua gốc toạ chừng.
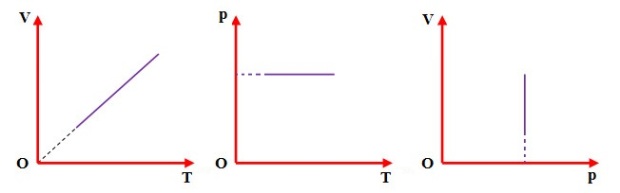
Đường đẳng áp trong những hệ tọa chừng (V,T), (p,T), (V,p).
IV. TỔNG QUAN CÁC QUÁ TRÌNH BIẾN ĐỔI CỦA KHÍ LÍ TƯỞNG
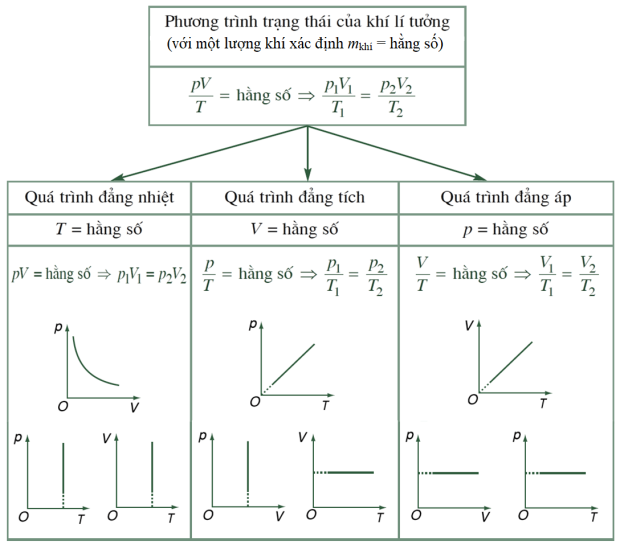
Phương trình tình trạng khí lí tưởng và những đẳng vượt lên trên trình
V. BÀI TẬP MẪU
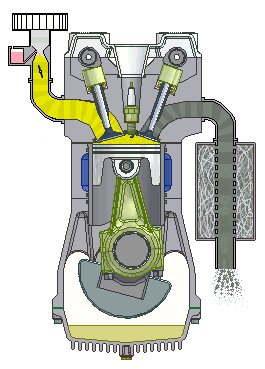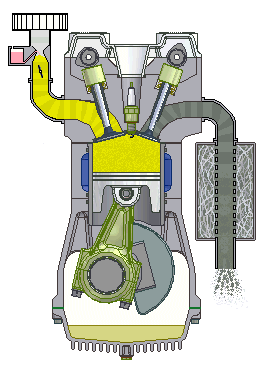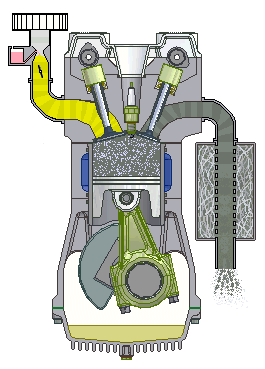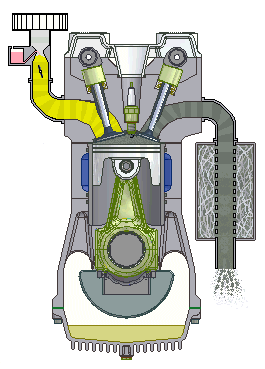
Động cơ nhóm nhập 4 kì
5.12. Trong xi-lanh của một mô tơ nhóm nhập, lếu hợp ý khí sở hữu áp suất 1 at, sức nóng chừng 47oC, thể tích 4 dm3. Nén lếu hợp ý khí cho tới thể tích 0,5 dm3 với áp suất 15 at. Tìm sức nóng chừng của khí sau khoản thời gian nén.
Tóm tắt
- Trạng thái 1 (khí trước lúc nén):
p1 = 1 at.
t1 = 47oC => T1(K) = t1(oC)+ 273 = 320 K.
V1 = 4 dm3.
- Trạng thái 2 (khí sau khoản thời gian nén):
p2 = 15 at.
V2 = 0,5 dm3.
t2 = ? oC
Áp dụng phương trình tình trạng khí lí tưởng:
Nhiệt chừng khí sau khoản thời gian nén:
Xem thêm: xo so, ket qua xo so, xsmb, xsmn, kqxs, xo so 3 mien nhanh nhat
t2 = T2 – 273 = 327oC.
5.14. Một lượng khí sở hữu áp suất 750 mmHg, sức nóng chừng 27oC và thể tích 76 cm3. Tìm thể tích của khí ở ĐK chuẩn chỉnh (0oC, 760 mmHg).
ĐS: 68,25 cm3.










Bình luận